Corps pur et mélange
Cette partie correspond aux notions nécessaires de la partie non traitée en début d’année.
Corps pur
- Une espèce chimique est un ensemble d’entités chimiques (atomes, molécules ou ions) identiques.
- Un corps pur est une substance (liquide, solide ou gaz) constituée d’une seule espèce chimique.
- L’eau distillée est un corps pur
Mélange
- Un mélange est une substance (liquide, solide ou gaz) constituée de
plusieurs espèces chimiques.
- Il est hétérogène si on observe plusieurs constituants.
- Il est homogène si on ne peut pas distinguer les constituants.
- L’eau minérale est un mélange d’eau et de minéraux
- L’air est un mélange en majorité composé de diazote et de dioxygène
Masse volumique
La masse volumique (notée ρ) correspond au rapport de la masse totale d’une substance (m) par son volume (V), soit
ρ = m / V
Mise en application
Quiz
Composition d’un mélange
Dans une éprouvette, on verse 8 mL d’eau distillée, 5 mL d’huile (acide oléique), et 2 mL d’éthanol.
- Faire un schéma de la situation.
- Calculer la masse introduite de chaque liquide.
- Après agitation du mélange.
- Expliquer pourquoi on observe plus que deux phases liquides.
- Calculer la masse volumique du mélange eau-éthanol.
- Déterminer si le mélange eau-éthanol se retrouve au dessus ou en dessous de l’huile. Justifier la réponse.
Identifier une espèce dans un mélange
Dans une salle de classe, du sulfate de cuivre anhydre et de l’eau de chaux ont été laissé à l’air libre. Au bout de quelques jours, la poudre blanche est devenue bleue, et le liquide limpide s’est troublé.
- En déduire deux espèces chimiques présentent dans l’atmosphère. Justifier la réponse.
Boissons sucrées
Toutes les boissons sont des mélanges constitués essentiellement d’eau et contenant plus ou moins de sucre.
Quel critère faut-il utiliser pour déterminer la boisson la plus sucrée ?
- Solution
- mélange homogène formé entre un solvant et un soluté
- Solvant
- espèce chimique majoritairement présente dans le mélange
- Soluté
- espèce chimique dispersée dans le mélange
| Boisson | 1 | 2 | 3 | 4 | 5 | 6 |
|---|---|---|---|---|---|---|
| Masse de sucre (en g) | 27 | 93 | 22 | 5,9 | 36 | 9 |
| Volume de la boisson (en mL) | 250 | 1000 | 500 | 200 | 330 | 420 |
| Masse totale de la boisson (en g) | 257 | 996 | 509 | 206 | 344 | 438 |
- Indiquer, dans les différentes boissons, quelle espèce chimique est le soluté, et quelle espèce chimique est le solvant.
- Calculer la masse volumique de chaque boissons.
- La concentration en masse correspond à la masse de soluté contenue dans 1 L de solution. Calculer la concentration en masse de sucre pour chaque boisson.
- Classer, à partir de la réponse précédente, les boissons de la plus sucrée à la moins sucrée.
À retenir
Une solution est un mélange homogène entre deux espèces chimiques, un solvant et un soluté.
Le solvant est l’espèce majoritairement présente dans la solution.
Le soluté est l’espèce chimique dispersée dans la solution.
Si le solvant utilisé est de l’eau, on parle alors de solution aqueuse.
La concentration en masse est définie par :
cm = m(soluté) / V(solution)
avec la masse de soluté en g, le volume de solution en mL, la concentration en masse cm s’exprime en g·mL-1.
- Lors d’une dissolution (ou dilution) la masse de soluté reste inchangée.
- Plus la concentration en masse de soluté augmente, plus la masse volumique doit augmenter.
Préparation d’une solution
Préparation d’une solution par dissolution
Pour préparer une solution de concentration en masse connue par dissolution, il faut choisir un solvant capable dans lequel le soluté peut se dissoudre.
Méthode pour préparer une solution de volume V de concentration en masse cm
Préparation d’une solution pour perfusion
Les poches de perfusion utilisées à l’hôpital permettent de réhydrater un patient et d’avoir un apport en nutriments. Un pharmacien doit préparer de manière la plus précise possible 50 mL de cette solution aqueuse contenant du saccharose.
Déterminer la masse de saccharose à prélever pour préparer 50 mL de solution.
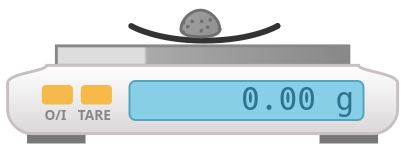
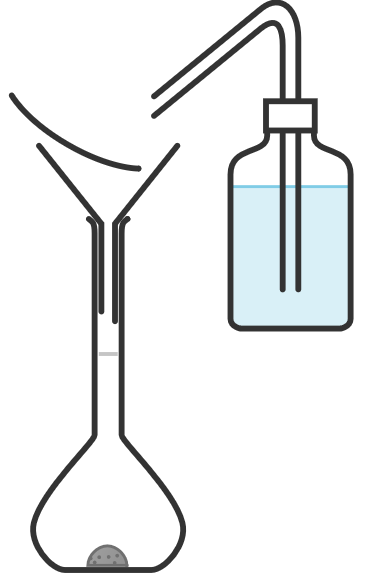
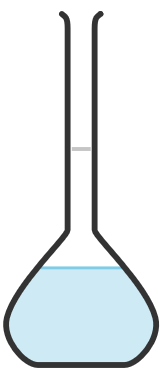
- Mesurer la masse de la fiole à vide, puis avec 50 mL d’eau.
- Calculer la masse volumique de l’eau.
-
Premier appel
Réaliser le protocole afin de préparer la solution.
Mesurer la masse volumique de la solution.
Préparation d’une solution par dilution
Solution de bleu brillant
Le colorant de bleu brillant E133 est un colorant alimentaire dont la consommation quotidienne ne doit pas dépasser la dose journalière admissible (DJA).
Comment préparer une solution de bleu brillant par dilution d’une solution mère ?
Objectif
Vous devez préparer 50 mL de solution de bleu brillant à partir d’une solution mère de concentration cm0 = 1,80 g·L-1. La solution à préparer doit représenter 3 % de la DJA après ingestion pour un enfant de 48 kg.
- Déterminer la masse de E133 correspondant.
- Déterminer la concentration en masse de la solution fille à préparer.
Conclusion
Conclure en faisant une remarque sur la couleur de la solution fille par rapport à celle de la solution mère.
Pour une solution colorée, plus sa concentration en masse de soluté est élevé, plus elle est foncé.
Il est possible d’utiliser la couleur d’une solution comme un indicateur de sa concentration en masse.
- On dissout un solide
- On dilue un liquide
À retenir
À savoir
- Une solution
- est un mélange homogène entre un solvant, espèce chimique majoritaire, et un soluté, espèce chimique minoritaire.
- La concentration en masse
- correspond à la masse de soluté contenue dans un litre de solution
- cm = m / V
- Dans une dilution
- la masse de soluté ne change pas
Savoir faire
- Savoir déterminer la concentration en masse, connaissant la masse de soluté et le volume de solution





Comment déterminer expérimentalement une concentration en masse ?
Un antiseptique efficace ?
La povidone iodée (ou bétadine) est un antiseptique d’usage local qui contient de l’iode.
Elle est utilisée pour l’antisepsie de la peau avant une opération, des plaies, des brûlures superficielles peu étendues et dans le traitement d’appoint des lésions de la peau et des muqueuses, infectées ou exposées à un risque d’infection.
Lorsque la solution est périmée, elle perd en efficacité.
Comment déterminer la concentration en masse d’une solution afin d’en vérifier son efficacité ?
Une échelle de teintes correspond à un ensemble de solutions, d’une même espèce chimique, diluée à partir d’une même solution mère colorée de concentration connue.
Ces solutions sont ensuite disposées dans des tubes à essais par ordre croissant (ou décroissant) de concentration en masse de soluté. Pour que l’échelle soit efficace il faut au minimum 4 solutions filles.
Cette échelle est généralement utilisée pour déterminer un encadrement de concentration en masse d’une solution.
Matériel
🤚 Premier appel
Réaliser l’échelle de teinte, puis indiquer un encadrement de la concentration en masse de la solution de concentration inconnue.
Combien de sucres dans mon soda ?
Courbe d’étalonnage
Une courbe d’étalonnage permet de déterminer graphiquement, une grandeur physique par mesure d’une autre.
Dans le cas présent, la variation de la masse volumique en fonction de la concentration en masse de soluté. Dans un premier temps, une série de mesures est effectuée pour établir le lien entre ces deux grandeurs. Dans un second temps, on mesure la masse volumique d’une solution de concentration inconnue, puis par lecture graphique, on détermine la concentration en masse.
Plus d’informations sur le site les manuels libres.
Ingrédients du soda
Par ordre décroissant de masse dans la solution :
eau gazéifiée, sucre, colorant E150d, acidifiant, acide phosphorique, arômes naturels, arôme caféine.
Données
Matériel