Caractéristiques d’un atome
La structure de l’atome
- Expliquer comment s’est construit la représentation de l’atome au fil des siècles.
- Faire un schéma de la représentation d’un atome selon le modèle de Schrödinger : nuage électronique, noyau, électrons, neutron, proton.
Un atome est une entité chimique composée d’électrons, et d’un noyau constitué de protons et de neutrons.
Il est électriquement neutre, il possède donc autant d’électrons dans son nuage électronique que de protons dans son noyau.
Écriture conventionnelle du noyau atomique
Le noyau d’un atome est représenté par l’écriture suivante :

Dans l’écriture conventionnelle du noyau, seules les informations sur le noyau sont données. On déduit le nombre d’électrons grâce à l’électroneutralité de l’atome.
Représentation du noyau du cuivre

Caractéristiques d’un atome
| Compétences | Notions |
|---|---|
| Utiliser les puissances de 10 | Masse des éléments d’un atome |
| Extraire des informations | Citer l’ordre de grandeur de la taille d’un atome |
| Argumenter | Effectuer le quotient de deux grandeurs pour les comparer |
Le graphène : un matériau d’avenir
Le graphène est un matériau bidimensionnel cristallin, composé exclusivement d’atomes de carbone 12 (12C). La structure cristalline est telle que chaque atome de carbone se retrouve au sommet d’un hexagone régulier de 0,14 nm de côté.
Quelques applications possible pour le graphène sont :
- électronique de très haute fréquence : les électrons se déplacent 150 fois plus vite dans le graphène que dans un semi-conducteur classique
- utilisation dans la construction de batteries : grande résistance mécanique permettant une grande durée de vie, finesse des feuilles permettant une grande surface d’échange permettant une charge plus rapide, et bonne conductivité.
- utilisation dans l’aéronautique, le graphène est eux cent fois plus résistant que l’acier et six fois plus léger.
D’après Wikipédia - Graphène

- Masse du neutron ou proton : mn = mp = 1, 67 × 10−27 kg
- Masse de l’électron : me = 9, 11 × 10−31 kg
- Calculer la masse du noyau d’un atome de carbone.
- Calculer la masse de l’atome en entier.
- Comparer ces deux valeurs et conclure sur la masse de l’atome.
Le noyau d’un atome de carbone mesure environ 1 fm = 10-15 m. Calculer le rapport entre les dimensions de l’atome et celle de son noyau.
Expliquer la phrase suivante :
L’atome est essentiellement constitué de vide.
- Un atome mesure près de 10-10m, son noyau mesure près de 10-15 m, soit 100 000 fois plus petit.
- Entre le noyau et le nuage électronique, il y a le vide.
Par comparaison, si le noyau avait la même taille que le Soleil, le nuage électronique serait plus loin que Neptune.
- La masse de l’atome est essentiellement due à la masse du noyau.
Exercices d’application
D’où viennent les propriétés chimiques d’un élément ?
Organisation des électrons dans le nuage électronique
Les électrons sont des particules élémentaires qui ne peuvent pas tous se situer dans les mêmes états d’énergie.
Comment sont répartis les électrons au sein d’un atomes ? En quoi cette répartition conduit à la stabilité de certains éléments ?
| Couche | Sous-couche | Nombre maximal d’électrons |
|---|---|---|
| 1 | 1s | 2 |
| 2 | 2s | 2 |
| 2p | 6 | |
| 3 | 3s | 2 |
| 3p | 6 |
- Sous-couche électronique
- correspond à un état d’énergie des électrons.
- Un atome est dans un état fondamental si les couches d’énergie les plus basses sont remplies.
- Couche de valence
- dernière couche électronique contenant des électrons
- Électrons de valence
- électrons situés sur la couche de valence
La classification périodique regroupe les éléments naturels et artificiels. Le site ptable.com permet de travailler de manière interactive avec un tableau périodique.
Configuration électronique
- Lithium
- 3 électrons : 1s2 2s1
- Oxygène
- 8 électrons : 1s2 2s2 2p4
Déterminer la configuration électronique des éléments suivant
- Aluminium
- Chlore
- Soufre
Expliquer ce que signifie l’électroneutralité d’un atome.
Déterminer le nombre maximal d’électrons possible sur une sous-couche de type s. Même question avec une sous-couche de type p.
Déterminer le nombre d’électrons dans l’atome suivant, puis déterminer son nom à l’aide de la classification périodique. 1s22s22p1
Compléter chaque case de la classification périodique suivante.
Colorier en vert les éléments dont la dernière sous couche remplie et en bleu ceux dont la dernière couche remplie est p.
Le cuivre dans tous ses états
Le cuivre est un élément chimique connu depuis l’Antiquité. Il est présent sous différentes formes au quotidien.
- Sous forme de métal pur, par exemple dans les fils électriques ou les tuyaux de plomberie. Le cuivre métallique se caractérise par sa couleur rougeâtre et sa grande conductivité électrique.
- Sous forme de ionique, comme le sulfate de cuivre (CuSO4 ), un composé bleu utilisé comme fongicide dans l’agriculture.
Quel lien peut-on établir entre ces différentes formes ?
- Pour chaque expérience, réaliser un schéma à l’état initial et à l’état final.
- Compléter le schéma suivant à chaque étape
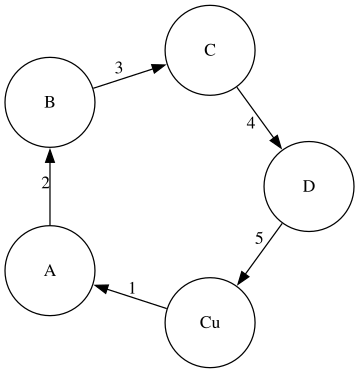
Action de l’acide nitrique sur le cuivre
L’acide nitrique est une solution très corrosive, cette manipulation doit être faite par votre enseignant sous la hotte.
Indiquer la couleur du métal cuivre et de la solution avant et après l’expérience.
Action de la soude sur la solution de sulfate de cuivre
Port des gants obligatoire
Protocole
- Mettre la solution de sulfate de cuivre dans un des tubes à essai
- Mettre environ 5 gouttes de soude dans le tube à essai
- Indiquer les réactifs de cette réactions.
- Compléter l’équation de réaction suivante : Cu2+ + ___ OH- → Cu(OH)2
- Filtrer la solution pour récupérer le solide B
Action de la chaleur sur le solide B
Protocole
- Récupérer le précipité et l’introduire dans un tube à essai
- Chauffer à l’aide d’un bec électrique le tube à essai jusqu’à disparition de la couleur bleu
Éviter au maximum l’ébullition pour éviter d’éventuelles projections
Compléter l’équation suivante : ___ + chaleur → CuO (s) + H2O (g)
Action de l’acide chlorhydrique sur le solide C
Protocole
- Verser quelques gouttes d’acide chlorhydrique sur le solide C jusqu’à disparition totale du solide noir.
- Ajouter de l’eau distillée pour remplir le tube à essai
D’après la couleur de la solution, indiquer l’espèce chimique obtenue.
Action du fer sur la solution D
Protocole
- Ajouter quelques copeaux de fer dans le tube contenant la solution D
D’après la couleur du dépôt sur les copeaux de fer, indiquer l’espèce chimique obtenue.
Classification périodique
Stabilité des éléments chimiques
Cas des gaz nobles
Les ions monoatomiques
Quelle eau choisir ?
En cas d’hypertension artérielle, il est recommandé de boire une eau riche en potassium, mais pauvre en sodium.
Parmi les trois flacons suivants, déterminer quelle eau est la plus adaptée pour une personne souffrant d’hypertension artérielle.
Concentration en masse des ions contenus dans 3 eaux minérales
| Ions | Formule | Eau 1 | Eau 2 | Eau 3 |
|---|---|---|---|---|
| Calcium | Ca2+ | 68 | 549 | 11,5 |
| Magnésium | Mg2+ | 7 | 119 | 8,0 |
| Sodium | Na+ | 11 | 14,2 | 11,6 |
| Potassium | K+ | 4 | - | 6,2 |
| Sulfates | SO42- | 5 | 1530 | 8,1 |
| Chlorures | Cl- | 19 | - | 13,5 |
| Bicarbonates | HCO3- | 234 | 383,7 | 71,0 |
| Fluorures | F- | 0,1 | - | - |
| Nitrates | NO3- | - | 4,3 | 6,3 |
Tests d’identifications
| Ion testé | Réactif testeur | Résultat |
|---|---|---|
| Calcium | Oxalate d’ammonium | Précipité blanc |
| Chlorures | Nitrate d’argent | Précipité blanc |
| Sulfates | Chlorure de baryum | Précipité blanc |
- Rédiger un protocole expérimental permettant d’identifier les eaux présentes dans les trois flacons.
- Mettre en oeuvre le protocole expérimental et noter vos résultats et schématiser les expériences.
- Répondre à la question posée en début d’activité. Justifier la réponse.
Les molécules
Énergie de liaison
L’énergie de liaison EAB entre deux atomes A et B dans une molécule correspond à l’énergie u’il faut fournir à la molécule pour rompre la liaison.
| Liaison | EAB (× 10-19 J) |
|---|---|
| H — H | 7,0 |
| N — N | 2,7 |
| O — H | 7,7 |
| O — O | 2,6 |
| O = O | 8,0 |
| C — C | 5,8 |
| C = C | 10,2 |
E(O2) = 7,30 × 10-19 J E(H2O) = 1,52 × 10-18 J E(CO2) = 2,65 × 10-18 J E(CH4) = 2,73 × 10-18 J
- Établir le schéma de Lewis des molécules suivantes : O2, H2O, CO2 et CH4.
- Calculer les énergies de liaison O = O, C — H, O — H, et C = O.
Exercices d’application
Composition des atomes
Reproduire, puis compléter le tableau suivant
| Élément chimique | fluor | ||||
|---|---|---|---|---|---|
| Numéro atomique | 5 | ||||
| Nombre de masse | 7 | 18 | |||
| Écriture conventionnelle | 28Si | ||||
| Nombre de protons | 3 | 11 | |||
| Nombre de neutrons | 12 | ||||
| Nombre de nucléons | 32 | ||||
| Nombre d’électrons | 16 |
Le silicium
Le silicium (Si) est un des éléments les plus abondants de la croûte terrestre. C’est un semi-conducteur notamment utilisé pour la fabrication des panneaux photovoltaïques.
La charge électrique de son noyau est 2,24 × 10-18 C, et sa masse est de 5,01 × 10-26 kg.
Déterminer l’écriture conventionnelle du noyau de cet atome.
- masse d’un nucléon
- mN = 1,67 × 10-27 kg
- charge élémentaire
- e = 1,60 × 10-19 C
Le chocolat
Le chocolat renferme plusieurs éléments bénéfiques pour la santé physique et mentale, comme le magnésium, le fer ou le potassium.
- Le magnésium (Mg) a pour numéro atomique Z = 12.
- Écrire sa configuration électronique.
- Déterminer la formule chimique de l’ion magnésium.
- Le fer (Fe) est absorbé par l’organisme sous forme de cations porteurs de deux charges électriques. Écrire la formule de l’ion fer.
- L’élément potassium (K) est situé dans la première colonne de la classification, en déduire la formule chimique de l’ion potassium.
Le fluor
Le fluor est un élément qui se trouve naturellement dans le fluorure de calcium, un solide ionique composé d’ions calcium et d’ions fluorures.
| Liaison | H — F | C — F | F — F | C — Cℓ |
|---|---|---|---|---|
| Énergie (× 10-19 J) | 9,4 | 8,1 | 2,5 | 5,5 |
- À partir de la position du calcium et du fluor dans la classification périodique, déterminer la formule des ions calcium et fluorures.
- Indiquer si ces ions sont des anions ou des cations.
- Les molécules fluorées les plus connues sont utilisées dans des
propulseur d’aérosol, comme le dichlorofluorocarbone
(CF2Cℓ2).
- Établir le schéma de Lewis de cette molécule.
- Déterminer l’énergie nécessaire pour rompre cette molécule.